Introducción
La reconstrucción de ligamento cruzado anterior (LCA) es actualmente uno de los procedimientos más frecuentes en cirugía ortopédica y traumatología. Sin embargo, a pesar de las actuales técnicas quirúrgicas, aún existe un grupo de pacientes en los que persiste una inestabilidad rotacional posquirúrgica. Aunque las causas detrás de esta inestabilidad pueden ser multifactoriales(1,2), la lesión del ligamento anterolateral (LAL), combinada con la ruptura del LCA, parece tener un impacto significativo(3,4). Aunque este tema continúa en debate(5), actualmente, muchos autores abogan por la existencia del LAL como una estructura anatómica como tal y por su rol biomecánico como un restrictor secundario que controla la rotación interna de la rodilla(6,7,8,9).
En los últimos años, a raíz de la descripción detallada de la anatomía y función de las estructuras anterolaterlaes de la rodilla(9,10,11,12), ha habido un creciente interés en desarrollar una técnica de reconstrucción anatómica del LAL como refuerzo suplementario a la reconstrucción del LCA, basado en el entendimiento de que la restauración de la anatomía normal conduciría a un resultado biomecánico óptimo, que consiga eliminar la inestabilidad rotacional residual y reducir el riesgo de fracaso de la plastia de LCA. Sin embargo, ha habido distintos estudios biomecánicos con resultados contradictorios(13,14,15,16), probablemente debido a variaciones en la técnica y descripción anatómica utilizadas.
Aunque aún no está definida una clara indicación, un reciente consenso de expertos(16) sugiere un algoritmo de indicación que incluye en este grupo de pacientes a aquellos pacientes con signos clínicos de hiperlaxitud, casos de revisión de roturas de plastia de cruzado, aquellos que practiquen deportes de alta demanda de mecanismo pivote (fútbol, baloncesto, rugby…) y aquellos que presenten grados elevados de pivot shift en la evaluación clínica. Asimismo, realizan una revisión de las distintas descripciones anatómicas reportadas en la literatura, con el objetivo de uniformar la nomenclatura y presentar una recomendación de técnica quirúrgica para la reconstrucción anatómica del LAL.
El propósito de este estudio es evaluar el rol del denominado ligamento anterolateral sobre la estabilidad rotatoria de la rodilla y el resultado biomecánico de la reconstrucción anatómica del mismo, combinado con la reconstrucción simultánea del LCA.
Material y métodos
Diez especímenes de rodilla de cadáver fresco congelado provenientes de donantes fueron obtenidos del banco de tejidos (media de edad: 65 años, 5 masculinos y 5 femeninos). Ningún donante presentaba historia de intervenciones quirúrgicas previas en la rodilla. Los especímenes se mantuvieron a una temperatura de –20 °C y fueron descongelados a temperatura de aire ambiente 24 horas antes de los experimentos. El fémur y la tibia fueron cortados en su diáfisis a 250 mm de la línea articular. Piel y tejido subcutáneo fueron resecados junto a las partes blandas más allá de 150 mm de la articulación. Se realizó una valoración de artroscopia inicial a cada espécimen para detectar la existencia de algún daño en los ligamentos cruzados u otra estructura intraarticular, en cuyo caso el espécimen sería excluido del estudio. Todos los procedimientos de disección y reconstrucción fueron realizados por el mismo cirujano. Asimismo, el proceso desde la preparación hasta la medición biomecánica se realizó en el mismo día para cada rodilla.
Evaluación biomecánica
La variable principal analizada fue la rotación interna de la tibia en respuesta a una fuerza de torque de rotación interna de 7 N-m, siguiendo como ejemplo estudios similares previos, y de este modo facilitar comparaciones posteriores. Cada espécimen fue colocado en un marco de fijador externo (Hoffman II Stryker) diseñado para permitir un rango de movimiento de 0° a 100°, y luego el marco fue fijado a una máquina de pruebas (Mecmesin Vortex-D) capaz de aplicar una fuerza de torque y medir la rotación con una precisión de 0,1°. La máquina fue programada para aplicar una fuerza de torque de rotación interna de 7 N-m sobre la tibia y reportar el máximo ángulo de rotación, mientras el fémur se mantenía firmemente asegurado. Las mediciones se realizaron en ángulos fijos de flexión de la rodilla de 0°, 30°, 60° y 90° para cada uno de cinco estados quirúrgicos de una manera secuencial: 1º rodilla intacta, 2º lesión de LCA, 3º lesión de LCA + lesión de LAL, 4º reconstrucción aislada de LCA y 5º reconstrucción de LCA + reconstrucción anatómica de LAL.
Técnica quirúrgica
Todos los procedimientos fueron realizados por el mismo cirujano ortopédico. Primero las medidas iniciales se documentaron en la rodilla intacta. Luego, el LCA fue resecado por artroscopia y se realizaron las medidas en la lesión de LCA. Posteriormente, mediante disección cuidadosa se identificó el LAL según la técnica descrita por Daggett y cols.(17). Se realizó una incisión profunda horizontal de 15 mm para liberar la inserción distal del LAL, situada en un punto intermedio entre el tubérculo de Gerdy y la cabeza del peroné, aproximadamente a 8 mm del cartílago articular tibial. De igual manera, se identificó y seccionó cualquier inserción de la banda iliotibial (BIT) al fémur distal, con precaución de no dañar el ligamento colateral lateral (LCL) durante la disección.
Reconstrucción LCA
La reconstrucción del LCA fue realizada por artroscopia utilizando un injerto autólogo de hueso-tendón rotuliano-hueso. Se estableció un portal anterolateral alto como portal de visión inicial. Luego, bajo visión directa, se creó un portal anteromedial alto parapatelar como segundo portal de visión para una mejor visión de la pared medial del cóndilo lateral. De la misma forma, bajo visión directa se creó un tercer portal accesorio anteromedial justo por encima de la línea articular medial situado 2 cm medial al tendón patelar, como portal de trabajo para el túnel femoral del LCA. El LCA nativo fue resecado con un sinoviotomo, dejando suficiente resto de muñón en cada lado para facilitar la identificación de las huellas de inserción. El centro de la huella fue marcado como el punto de inserción tibial y femoral. Se utilizaron las guías específicas (Acufex de Smith and Nephew) para crear los túneles femoral y tibial, y se fijaron los extremos óseos con dos tornillos interferenciales (Smith and Nephew), tensionando la plastia con la rodilla a 30° de flexión.
Reconstrucción LAL
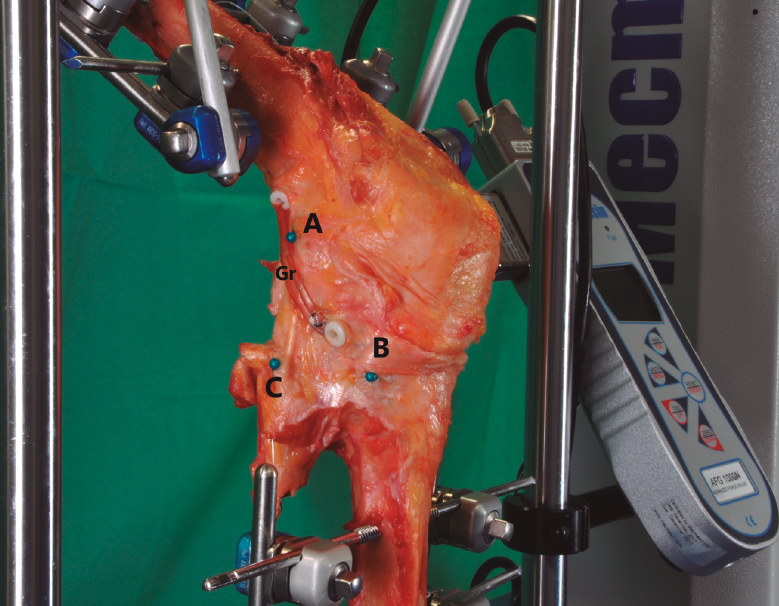
La reconstrucción del LAL se realizó utilizando un injerto autólogo de tendón de gracilis(16,18). Los puntos de inserción fueron localizados según referencias anatómicas. La inserción proximal en el fémur fue situada en un punto aproximadamente 4 mm posterior y 8 mm superior al epicóndilo lateral(11). La inserción distal en la tibia fue situada a la mitad de distancia entre el tubérculo de Gerdy y la cabeza del peroné, 10 mm distal al cartílago articular. La plastia autóloga de gracilis fue doblada en dos y suturada firmemente con puntos de anclaje en ambos extremos. Se crearon dos túneles óseos en las posiciones femoral y tibial mencionadas utilizando una broca canalada de 6 mm hasta una profundidad de 20 mm. La rodilla fue colocada en extensión completa para asegurar una rotación neutra y la plastia fue fijada en los túneles óseos mediante tornillos interferenciales (Smith and Nephew), manteniendo un trayecto superficial al LCL (Figura 1). Para la reconstrucción anatómica del LAL se utilizó la técnica descrita por el ALL Consensus Group(16), tensionando la plastia en posición de extensión de la rodilla, con el objetivo de evitar un efecto de sobreconstricción provocado por una excesiva rotación externa de la tibia(19,20).
Figura 1. Imagen de una rodilla derecha con las partes blandas resecadas para ilustrar la reconstrucción anatómica del ligamento anterolateral. A: epicóndilo; B: tubérculo de Gerdy; C: cabeza del peroné; Gr: plastia de gracilis.
Análisis estadístico
Para el procesamiento de datos y análisis estadístico se utilizó el programa SPSS (versión 23.3.3; IBM Corp.). Se calcularon la media y la desviación estándar para cada variable continua. Para confirmar la distribución normal de los datos utilizamos el test de Shapiro-Wilk. Se utilizó la prueba de análisis de varianza (ANOVA) para comparar las medias de las variables dependientes obtenidas de los datos de rotación interna de la tibia a lo largo de las variables categóricas independientes de estado quirúrgico y ángulo de flexión de rodilla. Las comparaciones post hoc de Tukey se realizaron al final. El valor de significación estadística se fijó en p < 0,05.
Resultados
Tabla 1. Rotación interna para cada estado quirúrgico y ángulo de flexión de la rodilla
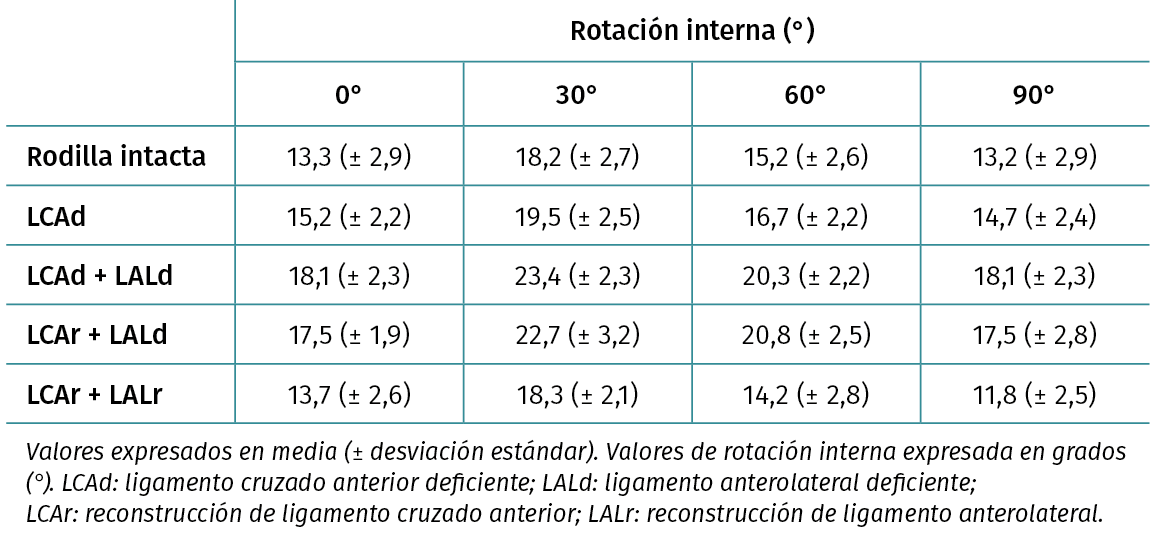
- Rotación interna de la tibia atribuible a la lesión aislada de LCA y a la lesión de LCA + lesión de LAL: la rotación interna en respuesta a una fuerza de torque de 7 N-m en una lesión aislada de LCA no tuvo un efecto significativo comparado con la rodilla intacta (p > 0,05), exceptuando un incremento significativo encontrado a 30° de flexión (p = 0,03). En la lesión combinada de LCA + LAL, se encontró un incremento significativo de la rotación interna respecto a la rodilla intacta en todos los ángulos de flexión examinados (p < 0,05) (Tabla 1 y Figura 2).
- Efecto sobre la rotación interna de la tibia de la reconstrucción aislada del LCA en presencia de una lesión combinada de LCA + LAL: después de realizar una reconstrucción de LCA, los valores de rotación interna de la tibia en respuesta a la aplicación de una fuerza de torque de 7 N-m mantuvieron un incremento significativo comparados con los valores observados en la rodilla intacta en todos los ángulos examinados (p < 0,05) (Tabla 1 y Figura 2).
- Efecto sobre la rotación interna de la tibia de la reconstrucción anatómica del LAL combinada con la reconstrucción del LCA en presencia de una lesión combinada de LCA + LAL: tras realizar una reconstrucción anatómica de LAL agregada a la ya realizada reconstrucción de LCA, los valores de rotación interna de la tibia en respuesta a una fuerza de torque de 7 N-m se restablecieron a los niveles de la rodilla intacta para los ángulos de 0° y 30° (p > 0,05). Respecto a los ángulos de 60° y 90°, se observó una reducción de la rotación interna (p < 0,05) interpretable como sobreconstricción, aunque la diferencia observada con respecto a la rodilla intacta fue relativamente pequeña (media de 3° ± 2° DS) (Tabla 1 y Figura 2).
Figura 2. Media de rotación interna de la tibia en respuesta a una fuerza de torque de rotación interna de 7 N-m. Cajas de 1 desviación estándar desplegadas sobre las barras. LCAd: ligamento cruzado anterior deficiente; LALd: ligamento anterolateral deficiente; LCAr: reconstrucción de ligamento cruzado anterior; LALr: reconstrucción de ligamento anterolateral.
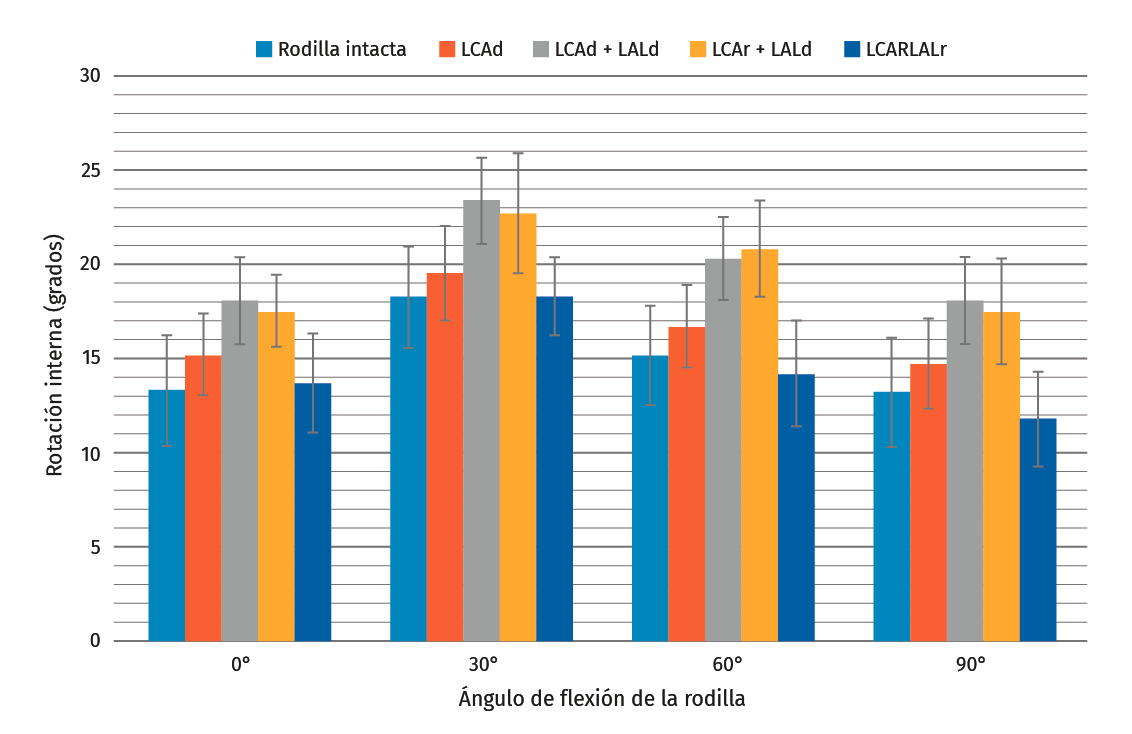
Figura 2. Media de rotación interna de la tibia en respuesta a una fuerza de torque de rotación interna de 7 N-m. Cajas de 1 desviación estándar desplegadas sobre las barras. LCAd: ligamento cruzado anterior deficiente; LALd: ligamento anterolateral deficiente; LCAr: reconstrucción de ligamento cruzado anterior; LALr: reconstrucción de ligamento anterolateral.

Discusión
El hallazgo más importante de este estudio fue que la lesión del LAL de la rodilla combinada con la ruptura de LCA produjo un aumento significativo de laxitud rotacional, que dicha laxitud rotacional fue persistente tras la reconstrucción aislada del LCA y que la reconstrucción anatómica del LAL fue capaz de restaurar los valores de rotación interna al nivel de la rodilla intacta.
Desde la publicación de Claes y cols. respecto a la anatomía del LAL en 2013(10), ha habido mucha controversia alrededor de su existencia y su rol en el control de la inestabilidad rotatoria de la rodilla en el contexto de una lesión del LCA. Numerosos estudios se han publicado, algunos promoviendo la importancia del LAL(7,10,11) y otros refutándola(21,22,23). En consonancia con nuestros resultados, algunos estudios observaron que la sección del LAL después de una rotura de LCA provocaba un incremento de la rotación interna de la tibia en fases tempranas de la maniobra de pivot shift(4,24). Otro estudio que realizó secciones seriadas mostró que el LAL solo entraba en acción cuando la rotación interna superaba los límites fisiológicos del LCA(21), concluyendo que el LAL es un estabilizador secundario que solo actúa ante la pérdida de función del LCA. Además, un estudio de diseño similar mostró que, cuando existe una lesión combinada de ACL + LAL, la reconstrucción aislada del LCA no es capaz de restaurar la cinemática normal de la rodilla(25).
Respecto a la reconstrucción anatómica del LAL, un estudio mostró que esta técnica tenía un efecto mínimo sobre la rotación de la rodilla(24). Sin embargo, la descripción anatómica utilizada en ese estudio fue vista como incorrecta, dado que la inserción femoral fue situada distal y anterior al epicóndilo en lugar de posterior y proximal. En contraste, un estudio anatómico demostró que la inserción femoral de la reconstrucción del LAL situada posterior y proximal al epicóndilo presentaba la mayor isometría con el menor cambio de longitud de la plastia durante el ciclo de flexión(26,27), confirmando lo descrito en la mayoría de estudios biomecánicos realizados(28).
La relevancia clínica de este estudio es que ayuda a determinar el rol biomecánico del LAL y la eficacia de su reconstrucción anatómica como un recurso ante los casos de laxitud rotatoria elevada o persistente en el contexto de una reconstrucción de LCA. Sin embargo, este tipo de estudios biomecánicos tienen las limitaciones del laboratorio, y se necesitan estudios clínicos con seguimiento prolongado para valorar los resultados.
Este estudio tiene ciertas limitaciones. Fue un estudio biomecánico en laboratorio con pruebas realizadas en el momento inicial que no puede evaluar los posibles cambios debido a las cargas cíclicas fisiológicas o al proceso de rehabilitación. Las lesiones del estudio, representando una lesión amplia de LCA asociada a LAL y BIT, fueron creadas quirúrgicamente. Esto no toma en cuenta la posible variabilidad de la lesión de acuerdo a la magnitud del trauma, pero el protocolo empleado permite una lesión reproducible para comparaciones homogéneas.
Conclusiones
La lesión del LAL de la rodilla provoca inestabilidad rotacional en presencia de un LCA deficiente. La reconstrucción aislada del LCA no consigue restaurar la estabilidad rotatoria en presencia de una lesión combinada de LCA + LAL. La reconstrucción anatómica del LAL, junto a la reconstrucción simultánea de LCA, es una alternativa efectiva para restablecer la estabilidad rotacional en caso de una amplia lesión anterolateral.