Introducción
Desde la reciente publicación de Claes(1) sobre el ligamento anterolateral (LAL), numerosos estudios han sido realizados con el objetivo de mejorar el conocimiento de esta estructura.
La primera mención a este ligamento fue realizada en 1879 por Paul Segond(2) al describir una “pearly, resistant, fibrous band” en la zona anterolateral de la rodilla causante de la fractura-avulsión de Segond. En décadas posteriores, múltiples nombres han sido utilizados para definir a esta estructura, “lateral capsular ligament”, “midlateral capsular ligament”, “midthird lateral capsular ligament” o “capsulo-osseous layer of the iliotibial tract”(3,4,5,6). El término ligamento anterolateral fue utilizado por primera vez en 2007 por Vieira et al.(7).
La inserción femoral de este ligamento es la que más discusión nos ofrece, con 3 localizaciones descritas(1,8,9,10,11,12,13,14,15): sobre el epicóndilo, proximal y posterior, y anterior y distal a este. La localización tibial ofrece menos discusión, situándola en la meseta tibial externa, entre en tubérculo de Gerdy y la cabeza del peroné.
Los estudios biomecánicos ponen de manifiesto el papel de esta estructura en el control de la estabilidad rotacional, existiendo debate sobre la posición donde se produce mejor función biomecánica por la misma. Parece ser que presenta mayor tensión en grados cercanos a la extensión(1,8,9,10,13,16,17), pero estudios recientes defienden su control a mayor flexión de rodilla(15,18,19,20,21).
Para el diagnóstico de esta lesión se ha puesto de manifiesto ser el causante del pivot shift en la exploración, aunque este concepto es controvertido(22,23,24,25,26). La fractura de Segond se puede justificar como una avulsión de este ligamento en su inserción tibial(9,27,28). La resonancia magnética (RM)(8,28,29,30) y la ecografía(31,32,33) están siendo utilizadas para caracterizar este ligamento.
Para su tratamiento se dispone de diversas técnicas de refuerzo extraarticular con diferentes tipos de injerto(34,35,36,37), obteniendo buenos resultados tras un seguimiento de 24 meses(38).
Debido a la gran cantidad de estudios con respecto a este ligamento en los últimos años, se cree conveniente realizar esta revisión bibliográfica para definir la incidencia, la anatomía, la biomecánica, la clínica, las pruebas de imagen y el tratamiento del mismo.
Metodología
Criterios de inclusión
Se incluyeron estudios descriptivos tanto clínicos como in vitro sobre las consideraciones anatómicas, biomecánicas, clínicas, estudios de imagen, manejo quirúrgico y resultados del LAL de la rodilla.
Estrategia de búsqueda
Se realizó una búsqueda en las bases de datos PubMed/Medline/Cochrane con los parámetros “(anterolateral ligament OR ALL OR lateral capsular ligament) AND (injuries OR anatomy OR biomechanics OR instability OR pivot shift OR Segond fracture OR MRI OR ultrasound OR reconstructions)”. Las consultas con expertos y la búsqueda manual de las referencias de los artículos fueron utilizadas para identificar estudios adicionales elegibles. También se incluyen los resúmenes de las conferencias organizadas por las siguientes sociedades: American Academy Of Orthopaedic Surgeons (AAOS), International Society of Arthroscopy, Knee Surgery and Orthopaedic Sports Medicine (ISAKOS) y European Society of Sports Traumatology, Knee Surgery and Arthroscopy (ESSKA). Se seleccionaron los estudios descriptivos hasta el mes de abril de 2017. También se incluyeron estudios publicados antes de su impresión.
Selección de estudios
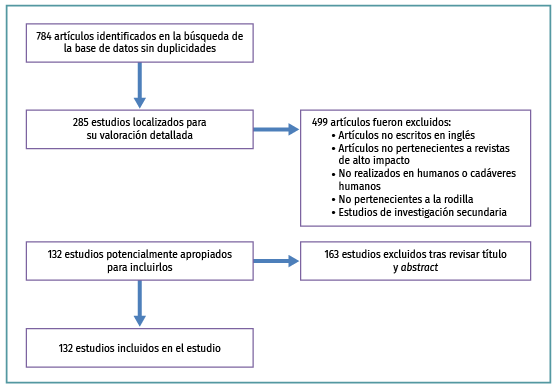
La estrategia de búsqueda expuesta anteriormente arrojó 784 estudios (Figura 1). Se realizó una selección manual de los artículos. Los criterios de exclusión fueron: artículos no escritos en inglés, publicados en revistas no indexadas, artículos de revisión, no realizados en humanos o cadáveres humanos y aquellos no pertenecientes a la rodilla fueron excluidos. Dos investigadores (AGC, DGG) excluyeron artículos tras revisar título y abstract. El desacuerdo sobre los datos y la inclusión del estudio se resolvió mediante discusión y consenso con un autor principal.
Figura 1. Criterios de selección de estudios.
Resultados
El número final de artículos seleccionados (132) fueron revisados para aclarar la incidencia, la anatomía, la biomecánica, la clínica, las pruebas de imagen, el tratamiento y la evolución del LAL. Los datos extraídos de los artículos fueron: tipo de estudio, fecha de publicación, autores, tamaño de la muestra, edad media, objetivo y resultados del mismo.
Incidencia y anatomía
El rango de prevalencia del citado ligamento en los diferentes estudios sobre especímenes cadavéricos humanos fue del 83-100%(22). Existe controversia en cuanto al origen extraarticular o intraarticular del mismo(8,9). Algunos reportan que la cápsula puede incorporar un número de fibras profundas del LAL(8,10,39), mientras que otros defienden el origen extracapsular del mismo(9,10,12,22).
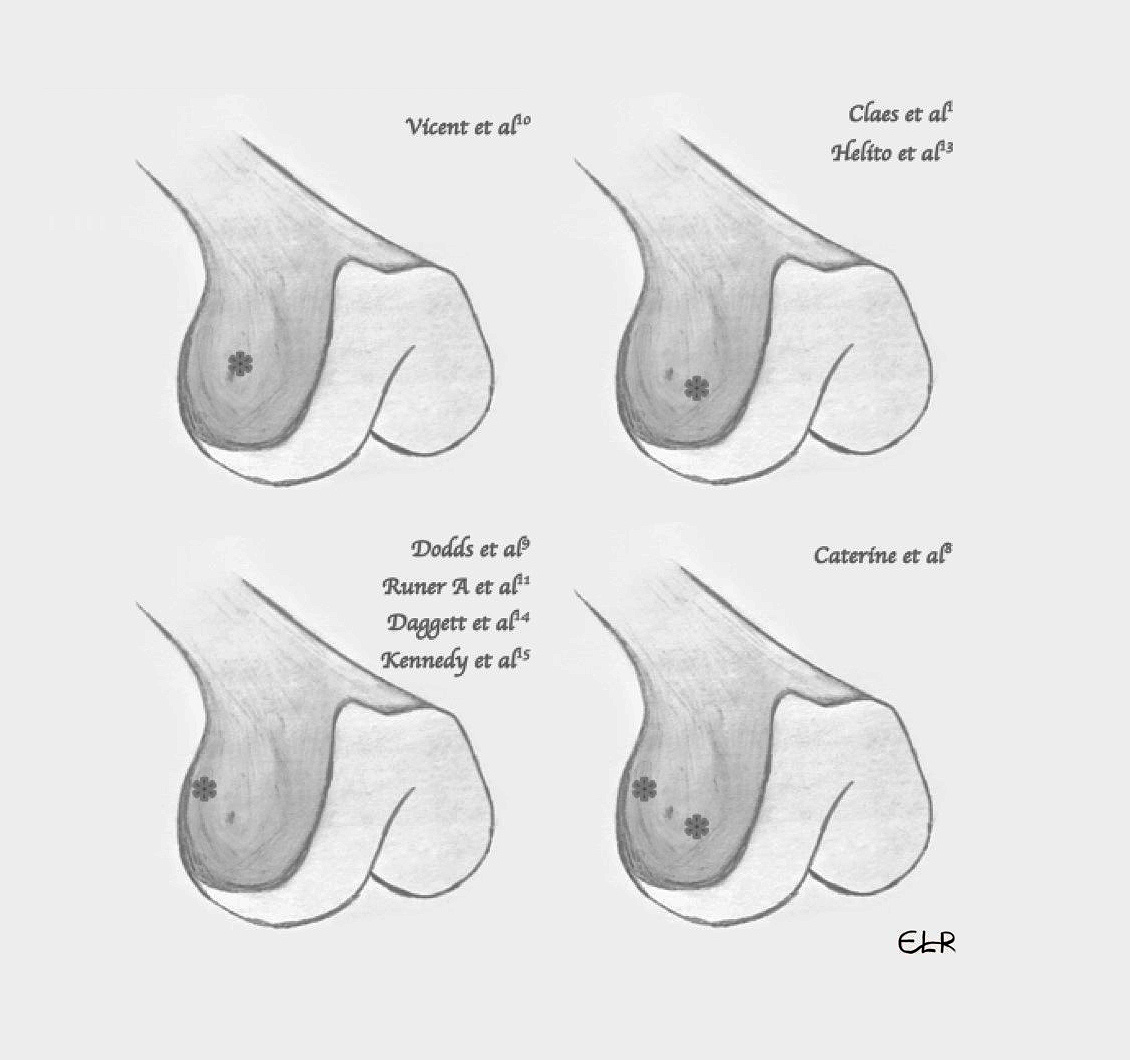
La localización de la inserción femoral es la que más discusión provoca. En el año 2012, Vincent et al.(10) realizaron 10 disecciones anatómicas de cadáver situando la inserción sobre el epicóndilo, anterior y distal al ligamento colateral lateral (LCL). En 2013, Claes et al.(1) y Helito et al.(13) situaron la inserción femoral de dicho ligamento anterior y distal al epicóndilo, anterior al LCL y proximal y posterior al tendón poplíteo en la mayoría de las 41 y 20 disecciones que realizaron, respectivamente. Al año siguiente, Dodds et al.(9) realizaron 40 disecciones, encontrando la inserción del LAL proximal y posterior al epicóndilo y al LCL. En el año 2016, Daggett et al.(14) localizaron en un estudio anatómico sobre 52 especímenes la inserción femoral con mayor frecuencia proximal y posterior al epicóndilo y LCL; posteriormente, de nuevo Claes(15) localiza la inserción en esta misma localización, no coincidiendo con su anterior publicación. Ese mismo año se publica un estudio de disección anatómica sobre 44 rodillas de cadáver(11), demostrando una inserción proximal y posterior al LCL. Catherine et al.(8) comprueban una inserción variable, posterior y proximal al LCL o anterior y distal al mismo. Aunque Stijak et al.(12) solo localizaron el ligamento en el 50% de las disecciones, su localización difiere de todas las anteriores. En todos los casos la unión del ligamento fue directamente al hueso(14)(Figura 2).
Figura 2. Origen femoral del ligamento anterolateral por los diferentes autores.
El trayecto del ligamento ha sido descrito de diferentes maneras. Dodds et al.(9) lo dirige en dirección oblicua (lateral a medial y proximal a distal) superfical al LCL; sin embargo, otros lo localizan profundo al LCL(1,10,12,13), presentando una fuerte conexión con el tercio medio del menisco externo(1,8,9,10,11,12,14,39,40), lo que podría explicar la asociación de lesiones del menisco externo asociadas al ligamento cruzado anterior (LCA)(41), presentes en el 44% de las reconstrucciones del LCA(42,43), con lesión de la raíz meniscal en el 23% de esas lesiones(42). Corbo et al.(41) demostraron que las fibras inframeniscales eran más fuertes y rígidas en comparación con las suprameniscales, presentando ambas la misma composición histológica. Van Dyck(44) et al. observaron que la mayoría de las lesiones se producían en la porción inframeniscal del LAL y que estos pacientes presentaban mayor riesgo de lesión meniscal lateral (61%), en comparación con los que no presentaban lesión del LAL (31%), sugiriendo que la lesión de estas fibras puede dar lugar a un menisco más móvil, soportando mayor tensión en la raíz posterior durante los episodios de subluxación anterolateral, provocando en consecuencia mayor riesgo de desgarro lateral del menisco. La inserción tibial ofrece menos dudas, localizándose en la mayoría de las ocasiones posterior al tubérculo de Gerdy(1), en la mitad entre una línea que une la cabeza del peroné con el tubérculo de Gerdy(1,8,9,10,11,39,40)(Tabla 1 y Figura 3).
Tabla 1. Prevalencia y localización del ligamento anterolateral (LAL)en los diferentes estudios
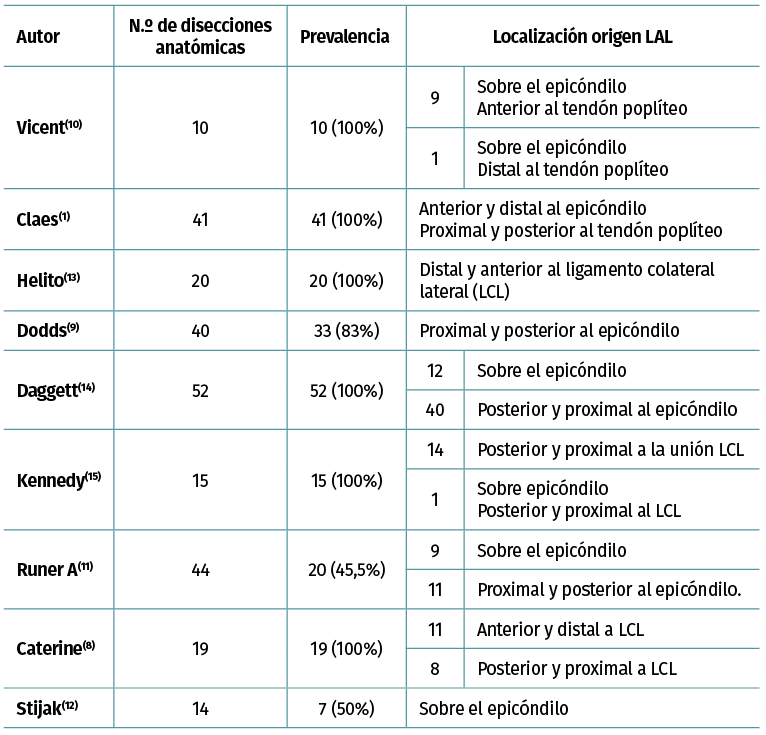
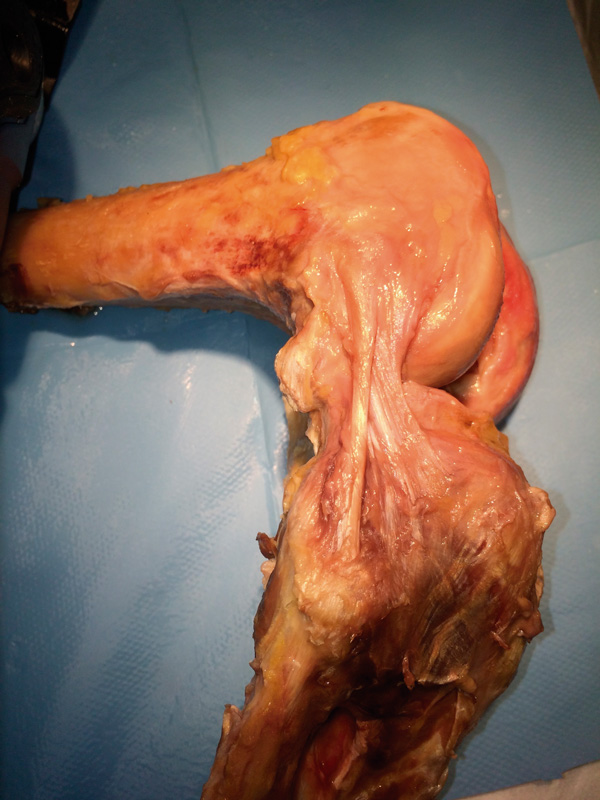
Figura 3. Disección anatómica de una rodilla humana derecha. Se aprecia la presencia del ligamento anterolateral (LAL) que discurre desde una inserción amplia en la región comprendida entre el tubérculo de Gerdy y la cabeza del peroné, pasa por debajo del ligamento colateral lateral (LCL) y se inserta en las proximidades del la inserción femoral del LCL, proximal y posterior a este.
La inserción femoral tenía una anchura media de 7,2-11,85 mm(1,11,14), mientras que la tibial de 11,2-12,2 mm(1,11). Las dimensiones del mismo son de 35 a 45 mm de longitud, 2 mm de anchura y de 1 a 2 mm de grosor(1,8,9,10), siendo tanto la longitud como el grosor mayores en varones que en mujeres(11,45). No se han apreciado diferencias en el peso del ligamento con respecto al sexo(45).
Biomecánica
En los últimos años existe mucho interés en las estructuras anterolaterales y la contribución de cada componente en la estabilidad rotacional de la rodilla.
En los años setenta, Hughston et al.(3), al describir el compartimento lateral de la rodilla, concluyeron que el “midthird capsular ligament” es el principal estabilizador lateral estático a 30° de flexión. En el año 2012, Monaco(23) et al. observaron en 10 rodillas cadavéricas intactas que la sección del LCA produce un leve aumento de la rotación interna, mientras que la sección de las estructuras anterolaterales produce un aumento significativo en todos los grados de flexión de la rodilla, sobre todo a 30°, contribuyendo también a la estabilidad anteroposterior. En su estudio inicial, Claes et al.(1) observaron que el LAL se encuentra completamente tensionado en flexión y rotación interna. En el estudio biomecánico de Ruiz et al.(16), se demostró que se produce un aumento de la rotación interna a 30° tras la sección del LCA y sobre todo de las estructuras anterolaterales, aumentando esta rotación si se producía la sección de ambos. Estos resultados estaban en consonancia con el estudio de Spencer et al.(18). El orden en que se realizaba la sección no influyó en la rotación resultante, por lo que se podía deducir que ambos ligamentos eran independientes y sinérgicos.
Parece ser que la localización femoral del LAL influye en la isometría del mismo. Zens et al.(19) y Kittl et al.(46) realizaron estudios biomecánicos en cadáver teniendo en cuenta la localización definida por Claes(1), anterior y distal al epicóndilo, y observaron un aumento de la longitud de manera uniforme desde la extensión completa hasta los 90° de flexión. Las rotaciones modificaban la longitud, aumentando la longitud en el caso de la rotación interna y disminuyendo en la externa.
Un estudio reciente realizado sobre 12 cadáveres(47) teniendo en cuenta las 3 localizaciones femorales más frecuentes reflejadas antes en la anatomía (epicóndilo, proximal y posterior a este, y distal y anterior al epicóndilo) observó que durante la rotación interna se produce un incremento de la longitud para las 3 localizaciones femorales a 20°, pero estaban significativamente aumentadas a 90°. La mayor longitud fue observada para la inserción posterior y proximal al epicóndilo y la menor para la anterior y distal al mismo. En este mismo estudio se comprobó que, si se mantiene la pierna en rotación neutra, se produce una disminución de la longitud en la localización proximal y posterior, y un aumento de la misma tanto en la posición anterior y distal como la situada sobre el epicóndilo. Si tenemos en cuenta que, en los primeros estudios biomecánicos(1,8,9,10,13,16,17), la función del LAL era el control de la rotación interna cerca de la extensión completa de la rodilla, podemos deducir que la localización posterior y proximal es la más isométrica teniendo un rango articular completo.
Los estudios biomecánicos más recientes ponen de manifiesto que el LAL es un estabilizador primario de la rotación interna de la rodilla a 35° o más de flexión con un mínimo rol en la estabilización anteroposterior(15,18,19,20,21). Dodds et al.(9) detectaron que el LAL es isométrico desde la extensión completa hasta la flexión de 60°, mientras que entre 60° y 90° apreciaron un acortamiento significativo, teniendo en cuenta su localización proximal y posterior al epicóndilo y la rotación neutra del miembro. Las rotaciones no producen cambios en la longitud con la rodilla en extensión completa, mientras que al pasar de 30° grados de flexión se produce un alargamiento del mismo, más significativo a 90°. Al realizar la rotación externa con la rodilla en flexión, se acorta. Estos hallazgos también fueron observados por Lutz et al.(20). Helito et al.(48) realizaron un estudio mediante tomografía computarizada para registrar los cambios de longitud en los diferentes grados de flexión y rotación de la rodilla, apreciando un incremento de la longitud desde los 0° a los 90°, presentando el mayor crecimiento desde los 60° a los 90°. En 2015, Parsons et al.(24), en un estudio biomecánico in vitro realizado sobre 11 rodillas cadavéricas, observaron que la contribución rotacional del LAL y el LCA a 30° eran similares, pero a medida que aumentábamos la flexión, la estabilización por el LAL era mayor, no teniendo ninguna función en la traslación anteroposterior de la tibia. Sonnery Cottet et al.(49) destacan el papel del LAL en el control de la rotación interna a 90° de flexión pero no a 20°, actuando conjuntamente con la banda iliotibial. Rasmussen et al.(17) demostraron biomecánicamente en un estudio robótico que la lesión conjunta del LCA y el LAL provoca una mayor inestabilidad rotacional en comparación con la lesión única del LCA desde los 0° a los 120° de flexión. Sin embargo, otros autores(50,51,52,53) defienden el papel secundario del LAL en el control de la rotación interna en rodillas con deficiencia del LCA, siendo el tracto iliotibial el principal restrictor a la rotación interna, aumentando su contribución a medida que aumentaba la flexión(49,50). En un reciente estudio biomecánico in vitro sobre 10 rodillas cadavéricas, Bonanzinga et al.(54) comprobaron que el LAL no influye en el control de la estabilidad anteroposterior, siendo el LCA el principal estabilizador tanto a 30° como a 90°. Sin embargo, sí se apreciaba un aumento de la rotación interna tanto a 30° como 90° tras la sección del LAL y un aumento en la aceleración del pivot shift test.
Puede ser que se haya infravalorado el papel de la banda iliotibial en el control de la rotación interna de la rodilla debido al enfoque en el LAL de los últimos años, tal y como aprecian Yamamoto(55) et al. y Hassler y Jacob(56), donde la resección de la banda iliotibial provoca un gran incremento de la rotación interna.
Clínica
La parte fundamental para un buen tratamiento de las lesiones ligamentosas de la rodilla es realizar un correcto diagnóstico. Dichas lesiones provocan cambios en la biomecánica de la misma favoreciendo su inestabilidad y su degeneración. Estos cambios en la estabilidad pueden ser identificados en la exploración física con los test específicos (anteroposterior Lachman test, varo-valgo stress test, dial test…); sin embargo, las exploraciones de otras estructuras ligamentosas, como el LAL, raíces meniscales, etc., no están bien establecidas.
Los estudios biomecánicos sobre el LAL más recientes ponen de manifiesto el control de la estabilidad rotacional a grandes ángulos de flexión(9,18,20,21,24,47,48,49), donde no existiría un pivot shift significativo (se explora a unos 30° de flexión), mientras que otros defienden el control del mismo en extensión y escasos ángulos de flexión(1,8,9,10,13,16,17), con posibilidad de ser apreciado en el pivot shift, siendo un restrictor secundario en la estabilidad anteroposterior.
La maniobra de pivot shift nos muestra una inestabilidad rotacional, existiendo debate entre las estructuras cuya insuficiencia es responsable de su aparición (LCA, LAL, banda iliotibial, raíz del menisco externo…) y el grado en que contribuye cada una(4,23,50,57,58,59,60,61). Así, varios autores han intentado esclarecer este concepto, analizando la alteración del LAL con el grado de pivot shift apreciado, demostrando que un alto grado de pivot shift está relacionado con la lesión de dicho ligamento(22,23,24,25,26). Song et al.(62) reportaron que, en el 78,7% de las lesiones del LAL objetivadas mediante RM en lesiones concomitantes al LCA, se apreciaba un pivot shift de grado II-III, al igual que en otras publicaciones(18,63,64).
Sin embargo, otros estudios(50,51,54,65), en los que se secciona el LAL, no encuentran un aumento significativo del pivot shift con un LCA intacto, obteniendo un mayor aumento de la rotación interna a 60° de flexión.
Ferreti et al.(66), en su estudio, analizaron el tipo de lesión en el compartimento lateral hallada durante la cirugía con el grado de pivot shift presente, sin obtener correlación entre el tipo de lesión y el grado de pivot shift encontrado; no obstante, en todos los casos con pivot shift de grado II o III, la reconstrucción ligamentosa del mismo reducía o hacía desaparecer el pivot shift.
Pruebas complementarias
Radiología simple
En 1879, Paul Segond describió una fractura-avulsión en la parte proximal externa de la tibia con la rotación interna forzada en rodillas cadavéricas humanas(2) debido a una banda fibrosa y resistente. Cien años después de la descripción de esta lesión, en 1979, se comenzó a asociar esta lesión con la presencia de inestabilidad en la rodilla(67).
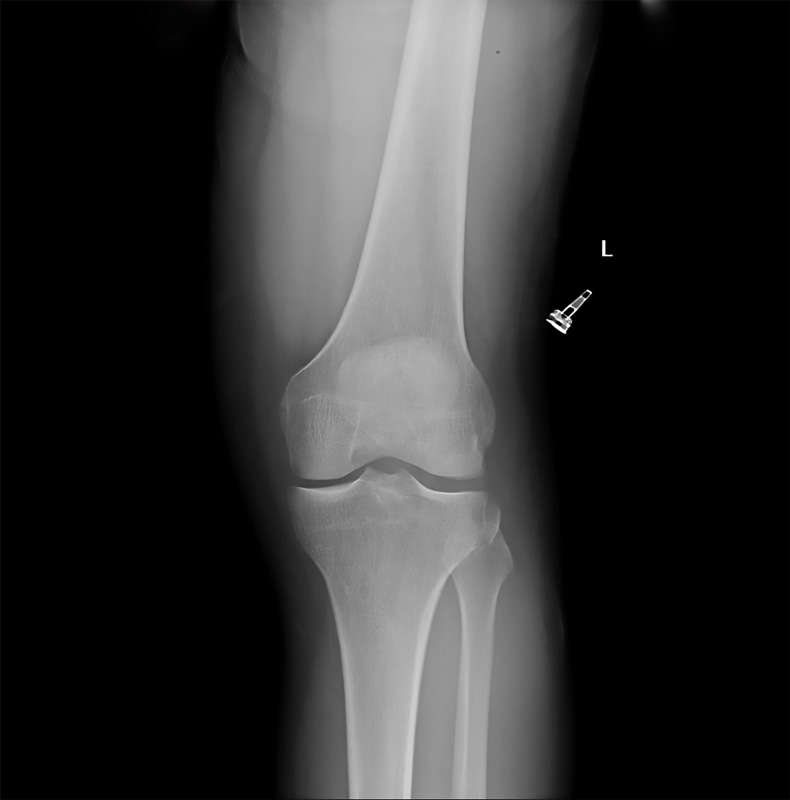
Clásicamente, se ha considerado a la fractura de Segond un signo patognomónico de la lesión del LCA en la población adulta(68,69,70). La localización de la inserción tibial del LAL posterior al tubérculo de Gerdy(1,8,9,10,11,39,40) y la frecuente combinación con la lesión del LCA hacen que se haya relacionado la lesión de esta estructura con la fractura de Segond(9,27,28). La banda iliotibial(5,68,69), la zona central de la cápsula articular(6,67), el brazo anterior de la cabeza corta del bíceps femoral(70) y la banda anterior del LCL(5,71) también han sido propuestos como causantes de esta lesión(72)(Figura 4).
Figura 4. Avulsión ósea en zona lateral de tibia proximal (fractura de Segond).
Ecografía
La ultrasonografía es una herramienta de diagnóstico fiable para identificar una estructura hiperecogénica en la zona anterolateral de la rodilla correspondiente al LAL(31,32,33). Además, permite un estudio dinámico de la misma. La fractura de Segond también ha sido diagnosticada en un alto porcentaje de las rodillas analizadas en comparación con la radiología simple o la RM(31,73), lo cual puede ser explicado por la posición en la que la exploración es realizada.
Resonancia magnética
La visualización del LAL mediante RM para poder realizar un diagnóstico conjunto con lesiones del LCA también ha sido estudiada. El primer problema que se encontró fue la dificultad para la identificación de este ligamento con los protocolos habituales de RM(29-74). Helito et al.(29) visualizaron el LAL en el 97% de los casos con una máquina de 1,5 T y cortes de 2,5 y 3 mm. Caterine et al.(8) pudieron apreciar las características de este ligamento en las 10 rodillas estudiadas, al igual que Porrino et al.(28), utilizando los primeros una maquina de 3 T y con cortes de 0,4 mm. Por su parte, Kosy et al.(30) identificaron la citada estructura en el 94% de las 100 rodillas estudiadas. Sin embargo, Taneja et al.(75) solamente pudieron observar la estructura en el 51% de las RM con un grosor de cortes de 3 mm.
Los estudios anteriores visualizan un ligamento sin alteraciones, aunque también ha sido estudiada mediante RM la posible afectación del mismo asociado a lesiones del LCA(44,76,77). La prevalencia de lesiones asociadas en el LAL cuando se encuentra el LCA roto varía entre 39,5 y 78,7% con mayor afectación de la inserción tibial del LAL(44,76), aunque Helito et al.(77) localizan por igual la lesión tanto en zona proximal como distal.
También se ha encontrado correlación entre disecciones anatómicas y estudio por RM(78).
Por el contrario, otros autores visualizan el LAL con una resonancia de 1,5 T y cortes de 4 mm, pero no con suficiente detalle para determinar si está alterado o intacto debido a sus dimensiones(79), al igual que sucede en el estudio de Devitt et al.(80), en el que utilizando una resonancia de 3 T no consiguen identificar en la mayoría de los casos la completa longitud del LAL tanto en rodillas sanas como en las que presentan rotura del LCA. En otro estudio no se consigue visualizar debido a la confluencia con el LCL y la banda iliotibial(28).
El análisis de la fractura de Segond también ha sido realizado por RM en diferentes estudios, aunque la prevalencia de la misma con esta prueba complementaria, al igual que con la radiología simple, es baja(44,76). En estudios recientes(44,76) se ha observado que la fractura de Segond solamente ha podido visualizarse en el 1,8% de las lesiones del LAL en uno de los estudios(76), en el 6,1% en otro(77) y en el 37% en el restante(44).
Tratamiento
El tratamiento de la inestabilidad anterolateral de la rodilla, puesto de manifiesto con la prueba diagnóstica del pivot shift, ha ido evolucionando a lo largo del tiempo con el objetivo de un mejor control del mismo. Hace varias décadas se comenzó a utilizar la tenodesis extraarticular aislada(81,82,83,84), controlando de forma efectiva la inestabilidad rotacional pero ejerciendo solamente un moderado control sobre la inestabilidad anteroposterior con resultados pobres a largo plazo. Además, se observó un aumento de cambios degenerativos en el compartimento lateral de la rodilla(85,86).
Posteriormente, se pasó a la reconstrucción intraarticular transtibial del LCA mediante fascículo único, convirtiéndose en el gold estándar, con una orientación más vertical de la misma, mejorando en este caso la inestabilidad anteroposterior, pero con resultados pobres en el control de la inestabilidad rotacional(87,88).
En un afán de mejorar este control rotacional se comenzaron a realizar reconstrucciones con doble fascículo del LCA(89,90,91). Los estudios biomecánicos comparativos entre ambas técnicas demostraron la superioridad de la doble banda(92,93), no apreciándose diferencias en cuanto a la estabilidad y la progresión a artrosis con respecto a la banda única, pero sí se pudo comprobar un menor índice de rotura de la plastia, con un periodo de seguimiento de 10 años(94,95). Otros inconvenientes con este tipo de intervención son la mayor dificultad técnica y los problemas en la cirugía de revisión de la misma, por lo que hoy en día ha perdido popularidad.
Actualmente el gold estándar es la reconstrucción del LCA con banda única en posición anatómica(96,97), demostrando unos resultados satisfactorios en la mayoría de los casos(98). A pesar de esto, en algunos casos persiste la inestabilidad rotacional, presentando los pacientes un pivot shift positivo tras la reconstrucción(99), relacionándose con peores resultados(100).
Hoy en día, con el objetivo de controlar este pivot shift residual, se está asociando en algunos pacientes técnicas de reconstrucción de las estructuras anterolaterales asociadas al LCA, usando diferentes estructuras como son la fascia lata(34), tendones de la pata de ganso(35), aloinjertos(36) e incluso injertos artificiales(37)(Figura 5).
Para conseguir una reconstrucción exitosa, la posición de la plastia es fundamental(23)(Figura 6). La malposición de los túneles y los cambios en la longitud con respecto al grado de flexión de la rodilla pueden llevar a un aumento de tensión en el compartimento lateral y la plastia, lo que degenera en un fallo de la plastia y degeneración en el compartimento lateral(19,23).
Figura 5. Reconstrucción del ligamento cruzado anterior (LCA) asociada a refuerzo lateral extraarticular.
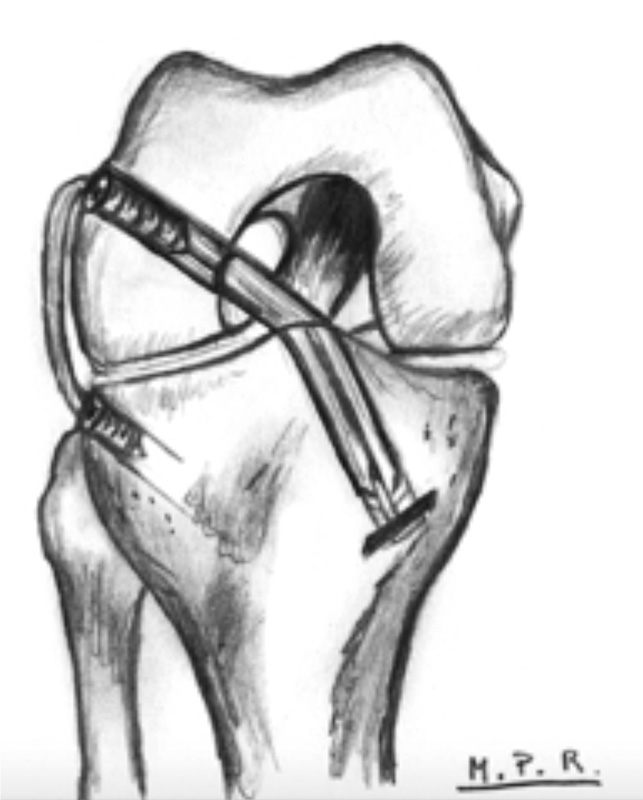
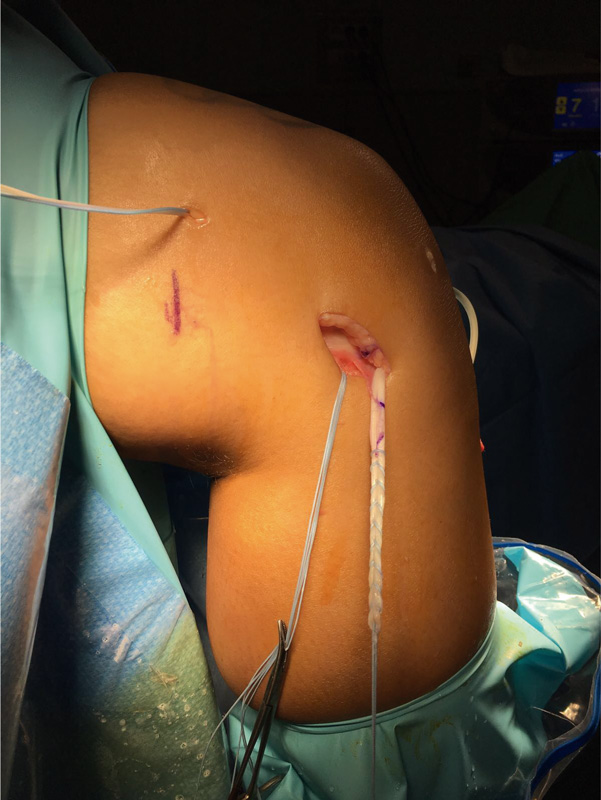
Figura 6. Imagen quirúrgica de una tenodesis extraarticular lateral de tipo Lemaire modificada. Nótese la presencia de los hilos de tracción de la plastia intraarticular anatómica del ligamento cruzado anterior (LCA).
La localización femoral del citado ligamento es la más discutida(1,3,4,5,7,8,9,10,11). En un estudio reciente, Kittl et al.(46) desarrollaron un estudio biomecánico registrando las variaciones en la longitud del ligamento utilizando las diferentes localizaciones del mismo con ángulos de flexión de 0° a 90° y determinan que la posición posterior y proximal al epicóndilo, pasando profundo al LCL y con fijación en extensión completa, era la más isométrica. Sin embargo, Katakura et al.(101) refieren que no hay diferencia entre pasar el injerto superficial o profundo al LCL.
Con respecto al tipo de injerto utilizado para la reconstrucción, la banda iliotibial tiene mejores propiedades biomecánicas en comparación con el tendón del gracilis(102,103).
Estudios recientes demuestran una disminución del pivot shift asociando esta reconstrucción del LAL a la cirugía del LCA(104,105,106). Mónaco et al.(107) demostraron una disminución del pivot shift con la utilización de una reconstrucción anterolateral asociada a la del LCA en comparación con la técnica de doble banda del LCA. La utilización de este refuerzo en cirugías de revisión del LCA también mejora la estabilidad de la rodilla(106).
Sin embargo, Anderson et al.(108) y Roth et al.(109) no encontraron ningún beneficio al añadir este refuerzo lateral, al igual que otro estudio actual(110).
Sonnery-Cottet et al.(38), en un estudio clínico prospectivo con 2 años de evolución, evidenciaron mejoría en los pacientes con esta plastia de refuerzo lateral tanto en estabilidad como en fallos y complicaciones.
Discusión
El control rotacional anterolateral de la rodilla es esencial para la estabilidad y la función de la misma. Clásicamente, ha sido considerado una parte fundamental del papel biomecánico del LCA(111), sobre todo del fascículo posterolateral del mismo; sin embargo, en los últimos tiempos su papel ha sido cuestionado(112) y otras estructuras han sido estudiadas para conocer su función en esta inestabilidad(4,23,50,57,58,59,60,61).
A pesar de que la mayoría de las reconstrucciones del LCA consiguen restaurar la normal traslación anteroposterior femorotibial, existe un elevado porcentaje de pacientes en los que persiste esta inestabilidad rotacional al no controlar el pivot shift(38,99,100).
Las técnicas quirúrgicas, el tejido empleado y los dispositivos de anclaje han ido evolucionando con el paso del tiempo en un intento de mejorar la función y controlar esta inestabilidad residual en algunos pacientes. Así, en 1916 se realizó la primera reconstrucción del LCA por Hey Groves de Bristol; posteriormente se pasó al uso de técnicas extraarticulares(81,82,83,84), no consiguiendo el control deseado en la estabilidad anteroposterior.
En las décadas de los ochenta y noventa se generalizó el uso de reconstrucciones intraarticulares, realizando en 1980 la primera reconstrucción artroscópica por David Dandy de Cambridge.
La técnica tradicional de 2 incisiones dio paso a una única incisión, realizando el túnel femoral a través del túnel tibial (técnica transtibial); sin embargo, algunos autores comunicaron la no posibilidad de colocar el injerto en posición anatómica, obteniendo una orientación más vertical de la misma(113,114). Por lo que se pasó a dar una orientación más oblicua a la plastia para mejorar el control de la rotación, situándola en posición de las 10 horas en lugar de las 11 horas(115), desde el portal anteromedial.
En un afán de mejorar la estabilidad proporcionada y restaurar la original anatomía del LCA, se pasó a técnicas de reconstrucción bifascicular(89,90,91), pero fueron abandonadas por no encontrar mejoría clínica con respecto a las monofasciculares(94,95) y ser técnicamente más demandantes, con peores soluciones en las cirugías de revisión.
Quizás porque la anatomía es demasiado compleja(116,117,118), es probable que sea imposible reproducir la anatomía fiablemente para que reproduzca la función del ligamento.
Por otro lado, la existencia de las estructuras anterolaterales es evidente(22) y su papel en el control de la rotación ha sido demostrado. Clásicamente, se pensaba que limitaba la rotación interna en grados cercanos a la extensión(8,9,10,16,17); sin embargo, otros estudios ponen de manifiesto una limitación rotacional a grados altos de flexión de la rodilla(15,19,21,49).
Dada la importancia del LAL en el control del pivot shift(62,63,64,66), se ha retomado el interés en las reconstrucciones de estas estructuras asociadas a la cirugía del LCA en un intento de disminuir el pivot shift residual y mejorar la estabilidad.
Recientemente, se ha publicado un estudio sobre la evolución de pacientes con reconstrucción anterolateral con buenos resultados(38), por lo que dejando a un lado la existencia o no del citado ligamento y la función del mismo, si se aprecia menor pivot, mejor función y menor índice de rerroturas, parece ser una buena opción de tratamiento. Actualmente, se encuentra en curso un ensayo clínico sobre la evolución de estos pacientes y podrá aclarar un poco más esta cuestión(119).
Aun así, con resultados prometedores en la reconstrucción anatómica del LAL, los resultados son a muy corto plazo, por lo que se deberían evaluar a más largo plazo, con estudios comparativos incluyendo las distintas variantes anatómicas femorales y comparando los resultados de reconstrucción del LCA junto al refuerzo lateral con la reconstrucción aislada del LCA.
Conclusiones
• La existencia del LAL de la rodilla es evidente.
• Su función principalmente es el control de la rotación interna, según parece, en grados cercanos a la extensión completa.
• Para su diagnóstico se dispone de la maniobra de pivot shift en la exploración, la fractura de Segond en la radiografía simple y otras pruebas complementarias como la ecografía y la RM.
• La reconstrucción de esta estructura obtiene resultados satisfactorios.
